Biomarqueurs
Des biomarqueurs non-invasifs, précoces et spécifiques pourraient se révéler très utiles pour une prise en charge efficace des maladies chroniques du foie et pour éviter les complications liées aux greffes de foie ou de rein. La prévention des maladies hépatiques et rénales est la meilleure stratégie à suivre pour éviter la transplantation. Ainsi, l’utilisation de stratégies diagnostiques ou prédictives précoces est cruciale pour identifier rapidement les patients atteints en vue d’une meilleure prise en charge clinique, pour réduire la morbi-mortalité associée à ces maladies très répandues et pour éviter ou retarder la nécessité d’une transplantation.
En greffe rénale, l’équipe P&T recherche des biomarqueurs urinaires de réactions de rejet du greffon, d’ischémie-reperfusion, de néphrotoxicité médicamenteuse et de dysfonctions tubulaires proximales.
Ces différents projets sont par essence multidisciplinaires et visent donc à développer de nouvelles approches diagnostiques et pronostiques pour améliorer la prise en charge clinique des patients atteints de maladies hépatiques ou rénales chroniques et des patients transplantés, en ouvrant la voie à des interventions thérapeutiques plus ciblées et personnalisées.
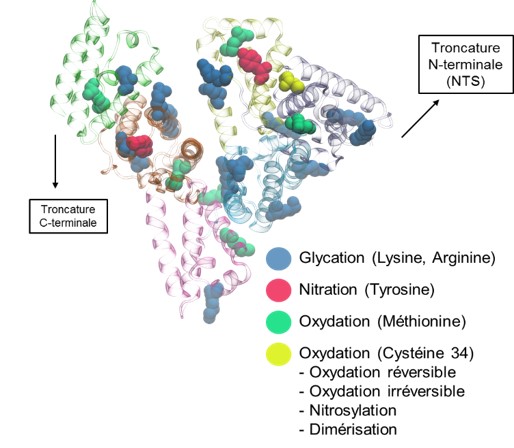
Les maladies hépatiques chroniques évoluent souvent de manière silencieuse, entraînant une stéatose, une fibrose voire une cirrhose avant que les patients ne ressentent des symptômes. Leur détection précoce est donc essentielle, en particulier pour les patients transplantés, car une prise en charge adaptée peut ralentir la progression de la maladie. Les biomarqueurs traditionnels comme les enzymes hépatiques (ALT, AST) et la bilirubine manquent de spécificité et n’apportent pas d’information quant à la nature des lésions hépatiques. Les modifications post-traductionnelles (PTM) de l’albumine sérique humaine (HSA) se présentent comme des biomarqueurs prometteurs, du fait de leur précocité et de leur spécificité.
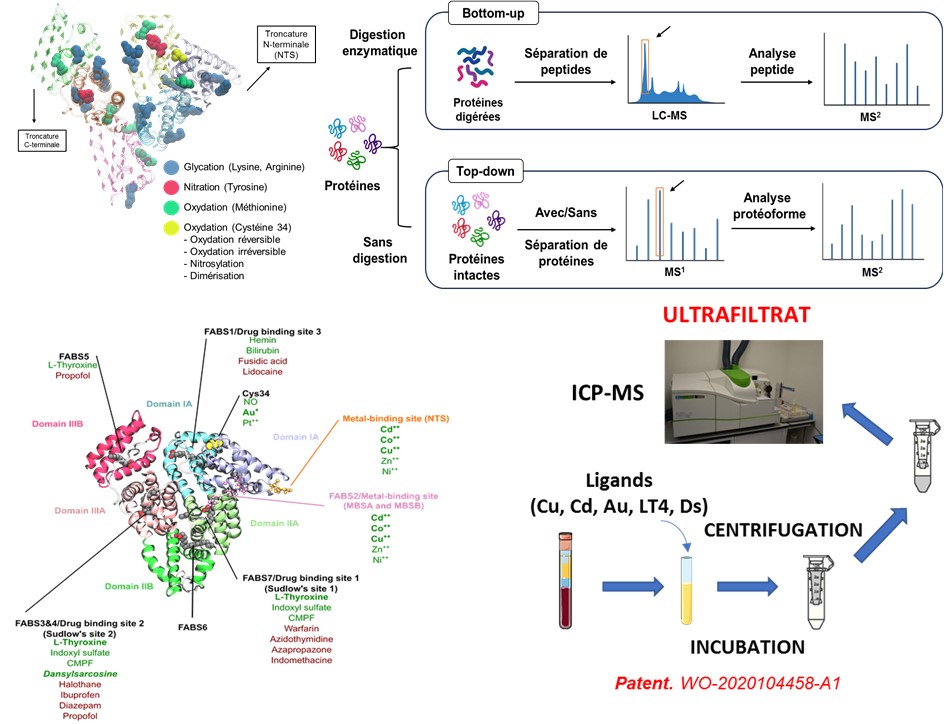
Notre recherche explore la détection et la quantification d’isoformes spécifiques de l’albumine comme indicateurs de lésions hépatiques. Nous avons mis au point le test « Serum Enhanced Binding » (SEB), qui détecte les changements structurels de l’albumine via des modèles de fixation de ligands mesurés par spectrométrie de masse. En recherche préclinique, cette méthode a permis détecter les dysfonctionnements hépatiques à des stades précoces.
Notre projet repose sur plusieurs approches : la chimie analytique pour caractériser les modifications de l’albumine, des études ex vivo sur lignées hépatocytaires pour comprendre les mécanismes des lésions, des modèles pré-cliniques pour suivre l’apparition des PTM, des études cliniques pour évaluer la valeur prédictive de ces biomarqueurs, des simulations in silico pour analyser les comportements de fixation, et une analyse des données par machine learning pour relier ces biomarqueurs à la nature et à la gravité de la maladie. Nous visons ainsi à améliorer le diagnostic des maladies hépatiques et des complications des greffes de foie, ouvrant la voie à des soins plus précis.
Pour pallier le manque d’organes disponibles en transplantation hépatique, le recours à des greffons dits « à critères étendus » devient assez courant. Ces greffons, bien que généralement viables, présentent des risques augmentés de dysfonction primaire ou de dysfonction précoce du greffon (EAD), une complication pouvant nécessiter une nouvelle greffe ou entraîner le décès.
L’objectif principal de ce projet est d’explorer les performances des PTM de l’albumine (HSA) comme biomarqueur très précoce, simple et fiable de la survenue de l’EAD, facilitant ainsi la prise en charge rapide des patients en échec de greffe hépatique. L’HSA est produite exclusivement par le foie et ses modifications post-traductionnelles (glycosylations et autres) semblent être différentes lors d’atteintes hépatiques. Les modifications post-traductionnelles de l’HSA peuvent donc constituer des indicateurs précieux de l’état du foie greffé au cours des quelques jours suivant la transplantation. En utilisant des techniques avancées de spectrométrie de masse haute résolution (LC-HR-MS), les variations et la répartition des isoformes d’HSA nous permettrons d’identifier les patients à risque de développer un rejet du greffon et d’améliorer ainsi la prédiction et la prise en charge des complications post-greffe. Le SEB test décrit plus haut sera également évalué dans cette indication, et adapté si nécessaire.
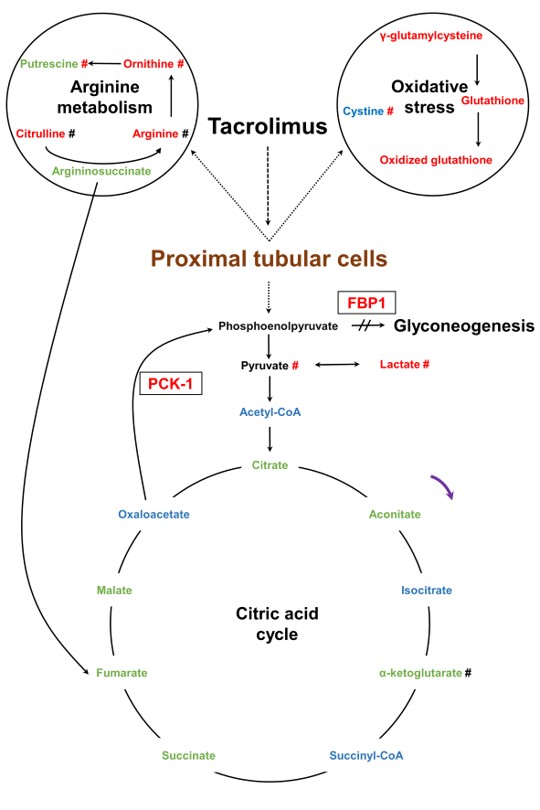
Le programme de recherche Européen BIOMARGIN (FP7 n° 305499) coordonné par P&T a déjà permis de détecter des biomarqueurs tissulaires et sanguins des réactions de rejet immunitaire contre le greffon. Les recherches concernant d’éventuels biomarqueurs urinaires, moins invasifs et plus accessibles, se poursuivent localement. Par ailleurs, après avoir étudié les mécanismes d’action néphrotoxique de la ciclosporine et du tacrolimus (Figure) par méthodes multiomiques, l’équipe s’intéresse maintenant à la néphrotoxicité potentielle de certains de leurs métabolites. En complément, un modèle combiné foie + tubule rénal sur puces est développé pour un autre axe de l’unité (intitulé ????) pour étudier la toxicité des métabolites médicamenteux produits par le foie, mais aussi l’influence d’interactions entre médicamenteux ou entre substances endogènes et médicaments sur les fonctions hépatiques et rénales.
Les transporteurs membranaires d’influx et d’efflux des tubules rénaux proximaux régulent l’excrétion et la réabsorption actives de nombreuses molécules endogènes et médicamenteuses. L’équipe a montré par le passé la vulnérabilité de ces transporteurs aux lésions d’ischémie-reperfusion liées à la transplantation. Dans le cadre de collaborations scientifiques dans et en dehors de la FHU SUPORT, la thématique évolue vers la recherche de biomarqueurs endogènes spécifiques des transports tubulaires, pour évaluer plus finement les lésions du tubule proximal, avec des applications anticipées dans la prise en charge des complications post-greffe précoces.