Les heptazines, de (relativement) nouvelles venues prometteuses en chimie moléculaire
Introduction
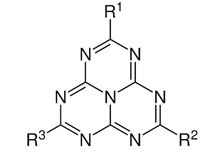
Fig. 1 : Formule générique des heptazines
La chimie des heptazines moléculaires est depuis peu l’objet d’un renouveau spectaculaire (Audebert et al., 2021). Les heptazines (un terme introduit dans les années 60 seulement, malgré des recherches bien plus anciennes), répondent à la structure générique ci-dessus (Fig. 1). La première synthèse d’une molécule attribuée à cette famille, longtemps rattachée à celle des nitrures de carbone, remonte à 1830 ; c’est par grillage du thiocyanate de mercure (les conditions de sécurité n’étaient pas alors ce qu’elles sont devenues de nos jours !), que le chimiste allemand Justus von Liebig obtient un solide jaune pâle qu’il nomme « melon ». Dans ce matériau, le cyle heptazine préexiste, et chacun des trois sommets substituables (R1, R2, R3 sur la Fig. 1) du cycle heptazinique porte une amine, mais les cycles sont oligomérisés (ce que forcément Liebig ignorait, le seul moyen de caractérisation à l’époque étant l’analyse élémentaire). D’autres synthèses analogues ont suivi et ont fourni par exemple le melem, une triaminoheptazine presque pure. Toutefois, pendant plus de 150 ans (!) seuls de rares dérivés d’heptazine ont été publiés, et la seule molécule à permettre l’extension à de nouveaux composés de cette famille de composés a été la trichloroheptazine (Kroke et al., 2002).
Toutefois, préparer la trichloro-s-heptazine reste très délicat. Il faut en effet chauffer à 140 °C du cyamelurate de potassium (sel de potassium de la trihydroxyheptazine, encore appelé acide cyamélurique) dans du pentachlorure de phosphore (PCl5), ou encore dans un mélange de PCl5 et de trichlorure de phosphore (PCl3). Ce sont des réactifs extrêmement agressifs et toxiques. La réaction produit également un peu d’acide chlorhydrique (HCl) gazeux et un peu de chlore. Pour effectuer cette réaction en sécurité, il faut donc disposer d’un équipement dédié, plutôt coûteux et que peu de laboratoires de recherche en chimie organique sont en capacité d’avoir. Résultat : Seulement très peu de laboratoires dans le monde produisent ou ont produit de la trichloro-s-heptazine. C’est un point qui a ralenti les recherches. Qui plus est, cette molécule est très réactive, s’hydrolyse rapidement avec l’eau atmosphérique, et pour finir n’est pas tellement soluble.
1. Propriétés des heptazines et état de l’art en synthèse
Les propriétés thermiques et chimiques de ces composés aromatiques affichant un squelette à trois hétérocycles azotés fusionnés ouvrent cependant la voie vers de nouvelles applications prometteuses, en particulier en optoélectronique et en photocatalyse, mais aussi celle de la préparation de COFs (Covalent Organic Frameworks) ou de MOFs (Metal-Organic Frameworks). Des travaux récents en chimie théorique du Pr W. Domcke montrent également que certaines de ces molécules, qui présentent toutes la particularité d’avoir une HOMO et une LUMO spatialement d’un recouvrement quasi-nul, sont susceptible de ce fait de violer occasionnellement la règle de Hund et ont dans certains cas un premier état excité triplet d’une énergie supérieure à celle du singulet !
Les heptazines sont souvent faiblement solubles voire insolubles. Toutefois le cycle heptazinique est cependant doté d’une haute stabilité thermique et chimique, se décomposant à des températures supérieures à 500 °C. Assez curieusement, cependant, les liaisons avec les substituants sont plus fragiles, et donc plus labiles que dans des cas proches comme les tétrazines ! Par exemple, en opposition avec les phosphotétrazines, les phosphoheptazines ne sont pas du tout stables (Schwarzer et al., 2013) : la liaison carbone-phosphore se casse spontanément en solution, pour on ne sait quelle raison. Les heptazines sont, malgré ces différences, toutefois assez similaires aux tétrazines en termes de réactivité et leur chimie fait majoritairement appel à des substitutions nucléophiles aromatiques.
Si les tétrazines fluorescent dans l’orange, les heptazines, elles, fluorescent dans le bleu-violet en général, mais leur couleur de fluorescence est plus dépendante des substituants et peul aller jusqu’au jaune-vert, car il s’agit d’une fluorescence traditionnelle basée sur une transition de type * (contrairement aux tétrazines qui utilisent une transition de type n-*) (Clavier et al., 2010). Cette fluorescence possède une longue durée de vie, car elle fait appel au mécanisme de type « fluorescence retardée thermiquement activée » (acronyme anglais TADF) à cause de la proximité des états singulet et triplet comme déjà mentionné. Cette caractéristique est très utile en photocatalyse car le substrat a le temps de diffuser vers le photocatalyseur. Elles sont également réduites quasi-réversiblement à un potentiel rédox relativement élevé. La présence d’un nombre important d’atomes d’azote dans les cycles aromatiques rend ces molécules très électro-déficitaires. Quand elles sont photo-activées, leur état excité est un oxydant fort.
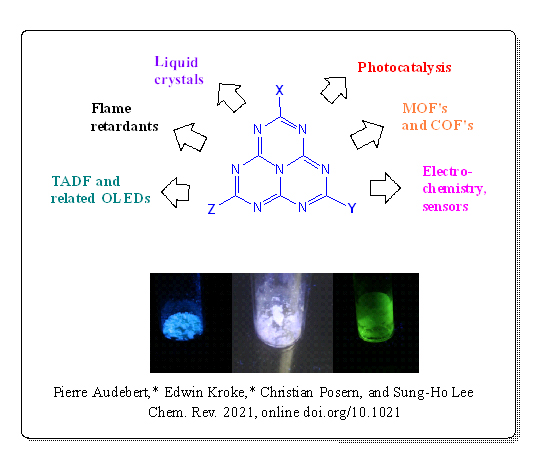
Fig. 2 : Rappel des applications potentielles des heptazines avec des images de fluorescence de quelques-unes d’entre elles (d’après la ref. 1).
Ces molécules présentent donc un comportement en spectroscopie et une affinité électronique élevée qui laissent entrevoir des applications prometteuses en optoélectronique et en photocatalyse. Alors que les photocatalyseurs actuellement utilisés sont majoritairement organométalliques, de ce fait occasionnellement toxiques et presque toujours coûteux, les heptazines pourraient fournir de nouvelles plateformes de catalyse photorédox efficaces et sans métaux. Nous venons tout juste d’avoir eu la chance de bénéficier d’un financement ANR accepté (Heptacat) en consortium avec le Dr G. Masson (ICSN, Gif s. Yvette) et le Dr F. Rossignol, à Limoges (IRCER) dont l’objectif principal est le développement de nouvelles familles de photocatalyseurs.
Egalement utilisées dans des applications industrielles en tant que retardateurs de flamme ou comme additif dans certains matériaux, les heptazines moléculaires ont longtemps fait un peu l’objet de recherches fondamentales, car le principal point névralgique pour leur production reste la synthèse, cela associé au fait que seule, jusqu’à il y a trois ans, la trichloroheptazine avait permis la synthèse d’un nombre important de molécules dérivées. Même si le melem a permis la synthèse de quelques dérivés d’heptazines isolés en suivant d’autre routes, toutes les autres voies de synthèse sont demeurées sans issue et n’ont permis la préparation que d’un ou deux composés isolés. Telle était la situation dans la chimie des heptazines avant notre découverte de la tris-(diéthylpyrazolyl)-s-heptazine.
2. La tris-(diéthylpyrazolyl)-s-heptazine ou TDPH, un acteur clé dans le renouveau de la synthèse des heptazines.
Notre nouveau précurseur - la tris-(diéthylpyrazolyl)-s-heptazine ou TDPH – (Galmiche et al., 2019), a permis pour la première fois d’éviter le passage quasi-obligé par la trichloro-s-heptazine et ainsi de contourner les inconvénients liés à sa synthèse. La TDPH présente plusieurs avantages : elle est bien soluble du fait des six groupes diéthypyrazole., on la produit simplement par mécanochimie (ou plus récemment par chimie au réacteur microondes) et mis à part un broyeur rotatoire à billes ou un réacteur à microondes, elle ne nécessite pas d’équipement spécial. On part de la mélamine pour obtenir, par pyrolyse, le melem, qui ensuite, par chauffage en présence d’hydrazine, donne la tris-(hydrazino)-s-heptazine, un solide quasiment insoluble à part dans l’eau acide (du fait des innombrables liaisons hydrogène présentes). Toutes ces étapes ne nécessitent aucune purification (qui serait d’ailleurs très difficile, ces molécules étant insolubles). Ce composé est en ensuite broyé en présence de la dicétone appropriée (la 3,5-heptanedione) et d’un catalyseur acide classique (APTS) pendant 15 minutes et obtient la TDPH avec un rendement de l’ordre de 30 %.
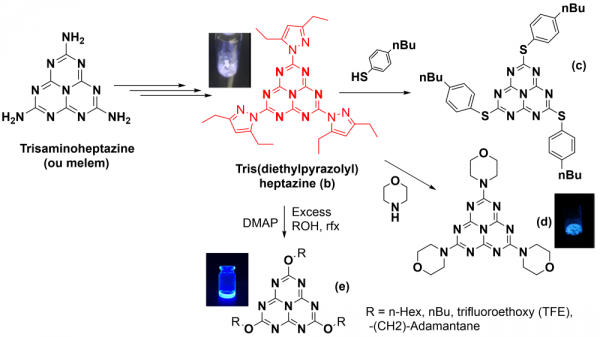
Fig. 3 : La TDPH et quelques exemples de sa flexibilité pour la synthèse de nouvelles heptazines.
La TDPH est un vraiment un synthon privilégié pour l’accès à de nouvelles heptazines. Quelques exemples de réactions très faciles à effectuer sont données sur la Figure 3 ci-dessus. La quasi-totalité des nucléophiles pas trop réducteurs (les réactifs de Grignard sont hélas une exception de nucléophile inadapté car trop réducteur) sont à même de substituer les pyrazoles qui font ainsi office de groupes partants facilement substituables.
Il est probable que les molécules issues de la TDPH permettent dans les années qui viennent de renouveler très positivement la chimie des heptazines, en permettant d’exploiter leur potentiel prometteur dans les directions précitées.
Conclusion
Sur la voie de sa maturité, la chimie des heptazines se montre désormais capable de se placer en bien meilleure position dans les recherches sur les molécules aromatiques hétérocycliques organiques actives. Il est loisible d’espérer une petite révolution dans le domaine de la photocatalyse, car aucun photocatalyseur purement organique ne possédant à ce jour l’ensemble des propriétés remarquables (haut potentiel rédox à l’état excité associé à un long temps de vie) de ces dernières. Dans les autres domaines ou les heptazines peuvent se révéler d’excellents candidats (typiquement l’électronique moléculaire et les fluorophores à fluorescence retardée), des plate-formes moléculaires existent (eg les phtalimides, ou les dicyanobenzènes) mais il n’est pas interdit d’espérer que là aussi, elles puissent permettre de dépasser les systèmes concurrents, bénéficiant en particulier de leur synthèse nécessitant moins d’étapes.