Plusieurs espèces de Digènes utilisent le mollusque Galba truncatula comme hôte intermédiaire pour le développement de leurs formes larvaires. Les cercaires, qui sont émises par la limnée, s’enkystent sur diverses plantes aquatiques comme le cresson. Si la liste de ces plantes hôtes est assez bien connue à l’heure actuelle, aucune information n’est, par contre, disponible sur la dispersion et la distribution de ces cercaires par rapport à l’espèce de la plante hôte. Des investigations ont donc été réalisées pendant trois années dans 14 cressonnières naturelles situées dans des rigoles de drainage superficiel et traversées par de l’eau courante. Dans chaque rigole, la population de G. truncatula vivait autour de l'émergence d'une source, tandis que la cressonnière était située plus en aval sur le cours même de la rigole. Cinq espèces végétales ont été récoltées au début du mois d'avril et examinées au stéréomicroscope pour y trouver des métacercaires. Des kystes appartenant à quatre Digènes : Calicophoron daubneyi, Fasciola hepatica, Notocotylus sp. et un Echinostomatidé non identifié ont été observés sur ces plantes. La plupart d’entre eux ont été observés sur Nasturtium officinale (243 sur 48,7 kg de feuilles et de tiges égouttées), suivis par Helosciadium nodiflorum (164 sur 33,4 kg). Sur les autres espèces végétales, il y avait peu de larves : de 18 à 25 par espèce. La plupart des cercaires de F. hepatica, de Notocotylus sp. et de l’Echinostomatidé se sont enkystées sur les feuilles supérieures et la zone des tiges situées juste sous la surface de l’eau, tandis que celles de C. daubneyi se sont fixées sur les feuilles basales et le collet des plantes. De plus, les plantes, sur lesquelles la plupart des cercaires se sont enkystées, poussaient dans la partie la plus en amont de chaque cressonnière (habituellement sur les premiers 50 cm de longueur). Lorsque l'eau courante dans les cressonnières était plus rapide, la distribution des métacercaires était plus limitée et leur nombre était inférieur à celui observé dans les stations alimentées par un lent débit d'eau. Les plantes qui poussent sur la section la plus en amont d'une cressonnière située dans une rigole de drainage superficiel sont les plus utilisées par les cercaires des quatre Digènes pour leur enkystement. La vitesse du courant d'eau affecte le nombre et la distribution des métacercaires dans une cressonnière.
Several species of Digenea use the snail Galba truncatula as an intermediate host for the development of their larval forms. Cercariae, which exited from the snail, encyst on various aquatic plants such as watercress. Although the list of these host plants is fairly well known at present, no information is available on the dispersion and distribution of these cercariae relative to the host plant species. Field investigations were therefore carried out for three years in 14 wild watercress beds located in open drainage furrows and crossed by running water. In each furrow, the population of G. truncatula lived around the emergence of a spring, while the bed was located further downstream on the course of the furrow. Five plant species were harvested in early April and examined for metacercariae using a stereomicroscope. Cysts belonging to four Digenea : Calicophoron daubneyi, Fasciola hepatica, Notocotylus sp. and an unidentified echinostomatid were observed on these plants. Most of these were observed on Nasturtium officinale (243 on 48.7 kg of drained leaves and stems), followed by Helosciadium nodiflorum (164 on 33.4 kg). On the other plant species, there were few larvae : from 18 to 25 per plant species. Most of the F. hepatica, Notocotylus sp. and echinostomatid cercariae formed cysts on the upper leaves and the area of stems just under the water surface, while those of C. daubneyi settled on the basal leaves and collar of the plants. In addition, the plants, on which most of these cercariae are encysted, grew in the most upstream part of each watercress bed (usually on the first 50 cm in length). When running water in the watercress bed was fast, the distribution of metacercariae was more limited and fewer in number than in the stations fed by a slow flow of water. Plants that grow on the most upstream section of a watercress bed in an open drainage furrow are the most used by cercariae of the four Digenea for their encystment. The speed of the water flow affects the number and distribution of metacercariae in the bed.
Introduction
Le cresson de fontaine ou cresson officinal (Nasturtium officinale R. Brown, 1812 in W.T. Aiton, 1812) fait partie des plantes potagères que l’homme utilise dans son alimentation. Cette espèce est connue pour sa richesse en vitamines, notamment en vitamine C, et pour ses sels minéraux (Van den Bruel, 1966 ; Grubben et Denton, 2004). Sa saveur un peu âcre est due à la présence de hétérosides sulfurés (glucosinolates) qui sont à l’origine du soufre présent dans la plante (Grubben et Denton, 2004 ; Schauenberg et Paris, 2016). Les caractéristiques particulières de cette plante aquatique expliquent en grande partie la culture de celle-ci dans des « cressonnières artificielles » constituées par des bacs ou des fosses parcourues par un courant lent et régulier d’une eau claire et peu acide (Matern et al., 2011 ; Virassamy, 2016). La réglementation française impose que cette eau ne provienne que de sources ou de puits artésiens. Elle exclut toute eau de surface, ainsi que des eaux de source qui, avant d’arriver dans les bassins, effectuent un long trajet ou un trajet à risque, par exemple, lors d’un passage par une pâture (Houin, 2009). Cette pratique culturale s’est essentiellement développée en France depuis 1810 avec une concentration des cressonnières dans le sud de l’Ile-de-France (Essonne). On assiste cependant à une diminution constante dans le nombre de ces exploitations depuis les années 1960 en raison de la désaffection des générations les plus jeunes pour cet aliment (Morizot, 2018).
Comme N. officinale pousse spontanément sur le territoire français en de nombreux points (https://www.tela-botanica.org/bdtfx-nn-43852-synthese), de nombreuses personnes dans le passé ont délaissé le cresson de culture commerciale produit dans les plantations agréées et ont consommé des échantillons de plante prélevés dans le milieu naturel. Ce « cresson sauvage » n’est cependant pas sans danger car les feuilles et les tiges sont parfois porteuses de stades larvaires de parasites (métacercaires). Le plus connu d’entre eux est Fasciola hepatica Linnaeus, 1758, à l’origine de la distomatose hépatique (« maladie de la grande douve du foie ») lorsque les métacercaires de cette espèce sont ingérées par l’homme ou les animaux (Taylor, 1965 ; Mas-Coma et al., 2018 ; Ortega and Sterling, 2018). La présence de ces parasites sur ce « cresson sauvage » fut à l’origine de plusieurs épidémies importantes de distomatose chez l’homme comme celle survenue en 1968 et 1969 dans les trois départements du Limousin (Rondelaud et al., 2000 ; Vignoles et al., 2019). Mais d’autres types de métacercaires ont également été identifiés sur ce cresson comme celles de Calicophoron daubneyi Dinnik, 1962 (« parasite de la panse des ruminants ») ou de Notocotylus sp. (Rondelaud, 2004). La présence de ces métacercaires est à l’origine de la mauvaise réputation que le « cresson sauvage » a dans la population et des mises en garde que de nombreux sites Internet diffusent sur le Web.
Lors d’une enquête épidémiologique sur les cas de distomatose humaine survenus entre 1970 et 2006 dans le Limousin, 252 points d’eau colonisés par N. officinale ont été identifiés (Rondelaud et al., 2009). Malgré leur superficie qui est réduite (< 2 m²) dans la plupart des cas, ces points d’eau ont été considérés par notre équipe comme des « cressonnières naturelles » (Rondelaud, 1978, 1980). Deux types de plantations, l’un dans les sites avec un sédiment vaseux et une eau stagnante et l’autre dans des endroits avec un sédiment sableux et une eau courante, ont été reconnus dans la Haute-Vienne. Selon le type de la plantation, la densité du cresson et les espèces végétales compagnes présentent des différences (Descubes-Gouilly et al., 1986). Les observations ultérieures effectuées par notre équipe dans ces sites ont porté essentiellement sur la recherche des métacercaires et leur dénombrement en relation avec la cressonnière et l’espèce de la plante hôte (Rondelaud et al., 2001 ; Rondelaud, 2004 ; Dreyfuss et al., 2005). D’après les études de Rondelaud (2004) et de Dreyfuss et al. (2005) sur les métacercaires de F. hepatica, la charge moyenne en kystes est faible (de 2,6 à 6,3 par site) dans les points d’eau colonisés par N. officinale en Haute-Vienne et l’on note une grande variation dans le nombre de ces cressonnières parasitées en fonction des années de l’étude. La distribution de ces métacercaires semble être indépendante de l’espèce de la plante hôte car Dreyfuss et al. (2005) notent un nombre sensiblement identique de kystes sur N. officinale et le faux cresson : 51,5 % sur N. officinale et 48,4 % sur Helosciadium nodiflorum (Linnaeus) W.D.J. Koch, 1824.
Malgré ces recherches, il reste encore des inconnues dans la contamination des cressonnières par les cercaires des parasites (Beesley et al., 2018). La question soulevée à plusieurs reprises par des consommateurs locaux de « cresson sauvage » était de savoir si tous les spécimens de N. officinale étaient porteurs de métacercaires dans le point d’eau où ces personnes effectuaient leur cueillette, ou s’il existait une zone préférentielle de la cressonnière naturelle dans laquelle les cercaires des Digènes s’enkystaient sur les plantes présentes. D’après Rondelaud et al. (2009) et Dreyfuss et al. (2015), les cercaires de F. hepatica émises par la limnée hôte s’enkystent sur les plantes les plus proches du mollusque lorsque l’eau de la cressonnière est stagnante. Mais nous n’avions aucune idée sur ce qui se passe lorsque la cressonnière est parcourue par de l’eau courante. Devant cette inconnue dans nos connaissances, 14 rigoles de drainage superficiel sur sols acides, colonisées par N. officinale ont été sélectionnées en avril-mai 2014 dans le nord de la Haute-Vienne et des investigations y ont été effectuées pendant trois années successives (2016-2018) afin de répondre aux questions suivantes : comment s’effectue la dispersion des cercaires de Digènes lorsque le cresson et les espèces compagnes sont situés en aval des mollusques dans un habitat parcouru par de l’eau courante ? Est-ce que l’enkystement des cercaires sur la plante hôte se produit dans toute la cressonnière ou seulement dans une zone préférentielle la plus proche du mollusque hôte ? Est-ce que les conditions pour l’enkystement des cercaires sont identiques pour les diverses espèces de parasites qui utilisent le cresson comme plante hôte ? Les trois années de l’étude se sont révélées nécessaires afin d’avoir des chiffres significatifs car la contamination des cressonnières naturelles par les cercaires des Digènes présente de grandes variations en fonction des années (Dreyfuss et al., 2004). Plusieurs données sur les métacercaires de F. hepatica ont déjà été publiées (Rondelaud et al., 2020). La présente note rapporte des informations non publiées sur F. hepatica et des données sur les métacercaires de trois autres Digènes que l’on rencontre dans les cressonnières naturelles sur sol acide.
Matériel et méthodes
2.1. Cressonnières prospectées
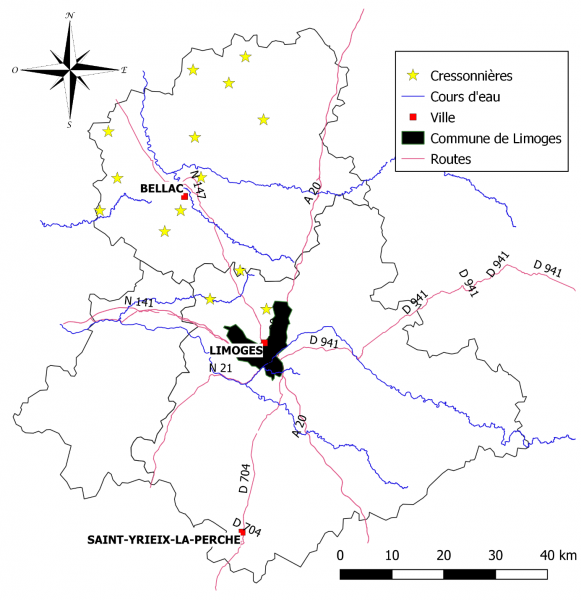
Figure 1 : Localisation géographique des 14 cressonnières naturelles dans le nord du département de la Haute-Vienne. Les limites administratives des trois arrondissements sont également indiquées sur cette figure.
Sur les 252 cressonnières naturelles recensées dans le Limousin, 14 d’entre elles ont été sélectionnées dans le nord de la Haute-Vienne. Il s’agissait de rigoles de drainage superficiel, situées dans des prairies marécageuses permanentes sur un sous-sol granitique (8 cas) ou gneissique (6 cas). La localisation de ces cressonnières dans le nord du département est précisée sur la figure 1. Le nombre de rigoles étudiées en fonction de leur type, de leur longueur, de leur superficie, de la vitesse du courant d’eau qui y circule et de la hauteur de celle-ci au début du mois d’avril est, d’autre part, fourni dans le tableau 1. Ces points d’eau ont été sélectionnés en raison des nombreuses métacercaires que notre équipe a décomptées sur le « cresson sauvage » entre 1990 et 2004 (Rondelaud, 2004 ; Dreyfuss et al., 2005). Dans les 14 prairies, la population du mollusque hôte : Galba truncatula (O.F. Müller, 1774), était répartie autour de l’émergence d’une source (à l’extrémité amont de la rigole) tandis que la cressonnière était localisée plus en aval sur le cours même de la rigole. La distance entre les limnées les plus excentrées autour de la source et le premier pied de cresson était différente selon les rigoles : de 0,1 à 0,3 m dans le cas de 5 rigoles, de 1,1 à 1,8 m pour 4 rigoles et de 3,0 à 3,5 m pour les 5 dernières (Tableau 1).
Tableau 1 : Caractéristiques principales des 14 cressonnières naturelles étudiées en 2016-2018 dans le nord de la Haute-Vienne. Leur localisation géographique est indiquée sur la figure 1.
|
Type de source et longueur de la zone sans macrophyte (m)* |
Nombre de rigoles |
Longueur de la cressonnière en m* (superficie en m²)* |
Eau courante (début avril) |
|
|
Vitesse (cm/s)* |
Hauteur (cm)* |
|||
|
Source à écoulement lent |
||||
|
0,13-0,24 |
3 |
6,6-9,2 (2,9-4,1) |
0,5-1,7 |
15,3-18,6 |
|
1,1-1,8 |
2 |
6,3-7,9 (2,8-3,5) |
0,9-2,1 |
14,7-17,2 |
|
3,1-3,5 |
2 |
7,8-9,5 (3,5-4,2) |
0,7-1,6 |
13,1-19,5 |
|
Source à débit plus rapide |
||||
|
0,15-0,29 |
2 |
6,4-6,9 (2,8-3,1) |
5,2-6,7 |
25,6-30,2 |
|
1,3-1,6 |
2 |
8,1-11,2 (3,6-5,0) |
4,3-7,2 |
22,1-26,7 |
|
3,0-3,2 |
3 |
9,3-12,2 (4,1-5,4) |
5,4-8,2 |
28,5-37,6 |
Deux types de rigoles ont été considérés dans ce travail en fonction de la vitesse du courant qui y circule (Tableau 1). Les sept rigoles du premier type étaient chacune alimentées par une source permanente ou temporaire, avec un écoulement lent. Leur largeur ne dépassait pas 45 cm pour une profondeur moyenne de 20 cm. Le sédiment était largement constitué par de la vase avec parfois du gravier et du sable. Les sept autres rigoles étaient chacune parcourues par de l’eau provenant aussi d’une source, mas avec un courant plus rapide. Leur largeur était identique à celle mentionnée ci-dessus pour le premier groupe, mais leur profondeur était plus grande : 30 cm en moyenne. A l’inverse des rigoles précédentes, le sédiment était principalement constitué par du sable, avec de rares plages de boue. Dans les 14 cressonnières, le pH de l’eau courante était compris entre 6,2 et 7, tandis que la concentration des ions calcium dissous était inférieure à 20 mg/L (Descubes-Gouilly et al., 1986 ; Guy et al., 1996). Les pieds de N. officinale y étaient peu nombreux et répartis sur le cours des rigoles. Par contre, d’autres macrophytes étaient présents dans ces cressonnières. En plus de N. officinale, notre étude a porté sur les espèces qui étaient les plus abondantes : H. nodiflorum (12 cressonnières), Juncus effusus Linnaeus, 1753 (11 cressonnières), Veronica beccabunga Linnaeus, 1753 (7 cressonnières) et Callitriche sp. (5 cressonnières). Les autres espèces végétales qui n’étaient représentées que par un ou deux pieds dans chaque cressonnière n’ont pas été étudiées dans le cadre de ce travail.
Dans le nord de la Haute-Vienne, le climat de type continental est fortement modulé par les vents humides qui proviennent de l’Océan Atlantique. Selon l’année, la pluviométrie annuelle moyenne varie de 800 à 1000 mm, tandis que la température annuelle moyenne varie de 3,1° C à 4,1° C en janvier et de 18,6° C à 19,3° C en juillet selon les municipalités (https://fr.climate-data.org).
2.2. Protocole des investigations
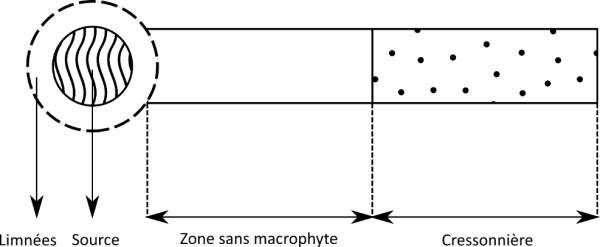
Chaque année, deux opérations ont été effectuées dans chaque cressonnière. Dans un premier temps, les quelques plantes présentes dans la rigole entre la population de G. truncatula et le premier pied de cresson ont été arrachées à la fin février afin de créer une zone exempte de macrophytes (Fig. 2) et d’éviter ainsi la fixation éventuelle des cercaires sur ces derniers. Comme les émissions cercariennes de G. truncatula ont lieu généralement à partir de la mi-mars (Rondelaud et al., 2009), la seconde étape a été effectuée au début du mois d’avril et a porté sur la récolte de cinq espèces végétales dans chaque cressonnière (Callitriche sp., H. nodiflorum, J. effusus, N. officinale et V. beccabunga) lorsque ces plantes sont présentes. Ces espèces ont été sélectionnées en raison de leur abondance relative dans ces rigoles (voir ci-dessus) et aussi des surfaces lisses que leurs tiges ou leurs feuilles présentent, ce qui permet une bonne adhésion des larves à la plante (Pécheur, 1967, 1974 ; Hodasi, 1972).
Figure 2 : Représentation schématique de l’extrémité amont d’une rigole de drainage superficiel étudiée dans le cadre de ce travail. Ce schéma montre la zone occupée par les limnées autour de la source, la zone sans macrophyte, d’étendue variable selon la rigole, et la cressonnière située plus en aval. Superficie de l’habitat avec Galba truncatula : de 1,2 à 1,7 m². Longueurs de la zone sans macrophyte et de la cressonnière : de 0,13 à 3,5 m et de 6,3 à 12,2 m par ordre respectif.
La vitesse du courant à la sortie de chaque cressonnière et la hauteur de l'eau ont d’abord été mesurées chaque année au début du mois d’avril grâce à deux relevés effectués entre 10 et 11 heures du matin avec un intervalle de trois jours entre les deux mesures. La distance entre le centre de chaque plante (avec une ou plusieurs tiges) et l'extrémité amont de la cressonnière a été déterminée dans un deuxième temps. La position de chaque plante par rapport à la largeur de la rigole de drainage a été précisée dans un troisième temps. Les parties submergées et parfois émergées de chaque plante ont été recueillies en coupant celle-ci au niveau du collet (sans les racines) et ont été introduites dans un sac individuel avec une étiquette indiquant l’espèce végétale et les valeurs des distances par rapport à l’extrémité amont de la cressonnière et la largeur de la rigole. Après leur transport au laboratoire, les tiges et les feuilles de chaque plante ont été placées pendant 12 heures à la température ambiante pour leur permettre de s'égoutter avant d'être pesées. Elles ont enfin été examinées au stéréomicroscope au grossissement x 4 ou x 10 afin d’y rechercher des métacercaires de F. hepatica ou celles d’autres Digènes fixées sur la plante. Comme la plupart des tiges et des feuilles (à l'exception de J. effusus) sont encore submergées au début du mois d'avril et que lesdites feuilles sont souvent dans un plan horizontal ou légèrement oblique, l'observation de chaque plante a été réalisée depuis l'extrémité supérieure de chaque tige et des feuilles correspondantes jusqu'au collet du végétal. Cette méthode nous a permis de noter i) le segment sur lequel chaque cercaire s'est enkystée et ii) la distance linéaire verticale entre le site de chaque enkystement et un plan horizontal passant par la base du végétal (zone du collet).
Comme Rondelaud (2004) et Dreyfuss et al. (2005) ont effectué leurs recherches dans le même type de cressonnières naturelles sur sols acides, les métacercaires fixées de quatre Digènes : C. daubneyi, F. hepatica, Notocotylus sp. et un Echinostomatidé (Echinostoma sp. ?), ont été recherchées sur ces plantes. Les critères morphologiques permettant d’identifier ces larves ont déjà été fournis dans deux synthèses sur G. truncatula (Rondelaud et al., 2009 ; Dreyfuss et al., 2015). Les quelques métacercaires flottantes observées sur ces plantes (Esclaire et al., 1989 ; Vareille-Morel et Rondelaud, 1991 ; Vareille-Morel et al., 1993), reconnaissables à la collerette autour de chaque kyste, n’ont pas été retenues dans le cadre de ce travail en raison des difficultés pour identifier l’espèce du Digène. Aucune étude en biologie moléculaire n’a été effectuée sur ces métacercaires, qu’elles soient fixées ou flottantes.
2.3. Paramètres étudiés
Les valeurs individuelles relevées pour les métacercaires dans chaque type de cressonnière (avec un écoulement lent de l’eau ou avec un courant plus rapide) au cours des trois années de l’enquête ont été regroupées afin d’obtenir des chiffres assez élevés car le nombre de métacercaires est généralement faible dans les cressonnières naturelles du Limousin (Rondelaud, 2004 ; Dreyfuss et al., 2005).
Les deux premiers paramètres sont le poids total des plantes pour chaque espèce végétale après un égouttement de 12 heures à température ambiante et le nombre de métacercaires identifiées pour chaque espèce de Digène. Leur étude a été réalisée en trois temps :
-
(i) La distribution de ces larves a d'abord été analysée par rapport à chaque espèce végétale. Le test exact de Fisher a été utilisé pour analyser la distribution des diverses catégories de métacercaires dans les deux types de cressonnières pour chaque espèce végétale, tandis que la fonction Fisher.multcomp du package RVAideMemoire (R Core Team, 2016) a été employée comme test post-hoc afin d’effectuer des comparaisons par paires. Nous avons également étudié la charge en métacercaires de F. hepatica et celle de C. daubneyi pour un kg de plantes égouttées afin de déterminer quelle était l’espèce végétale que les cercaires utilisaient le plus pour s’enkyster. Cette étude a été effectuée sur l’ensemble des métacercaires sans tenir compte du type des cressonnières. Les valeurs individuelles ont, dans ce cas, été d’abord analysées à l'aide du test de normalité de Shapiro-Wilk (Shapiro et Wilk, 1965). Comme la distribution de ces valeurs n'était pas normale, le test de Kruskal-Wallis a été utilisé pour établir des niveaux de signification statistique.
-
(ii) La distribution des métacercaires par rapport au segment végétal sur lequel chaque cercaire s’est enkystée a été étudiée dans un deuxième temps. Les valeurs notées dans les deux types de cressonnières ont été regroupées pour cette étude. Les kystes ont été classés dans l’une ou l'autre des catégories suivantes : face supérieure des feuilles, face inférieure des mêmes feuilles, tiges de la plante.
-
(iii) Le même protocole a été utilisé dans un troisième temps pour étudier la hauteur des sites, où les cercaires se sont enkystées, par rapport au collet de chaque plante. Les valeurs individuelles ont été classées dans l'une ou l'autre des catégories suivantes : 0-5 cm, 5,1-10 cm, 10,1-15 cm, 15,1-20 cm et > 20 cm.
Le troisième paramètre est la distance relative entre chaque plante porteuse de métacercaires et l'extrémité amont de chaque cressonnière. Cette dimension a été exprimée sous forme de sections longues de 50 cm afin de classer ces larves par rapport à la position de chaque plante. Le dernier paramètre concerne la position de chaque plante par rapport à la largeur de la rigole de drainage (45 cm) et a été exprimé sous forme de sections larges de 15 cm. Ces distances ont été calculées pour l’ensemble des métacercaires car nous n’avons pas constaté de différence nette dans les deux types de distances par rapport à l’espèce du Digène. Les valeurs individuelles notées pour chaque paramètre ont été ramenées à une moyenne, encadrée d’un écart type, en tenant compte du type de cressonnières et de la longueur de rigole sans macrophyte, située entre les limnées les plus excentrées de la population et le premier pied de cresson situé en aval. Ces valeurs ont été analysées à l'aide du test de normalité de Shapiro-Wilk (Shapiro et Wilk, 1965). Comme les distributions de ces valeurs n'étaient pas normales, le test de Scheirer-Ray-Hare, complété par le test post-hoc de Siegel et Castellan, a été utilisé pour établir les niveaux de signification statistique. Toutes les analyses ont été effectuées à l'aide du logiciel R 3.3.0 (R Core Team, 2016).
La nomenclature utilisée pour les plantes est celle que le Muséum National d’Histoire Naturelle de Paris a adoptée pour la dénomination de ces cinq espèces végétales (https://inpn.mnhn.fr/accueil/recherche-de-donnees/especes).
Résultats
Le nombre total de métacercaires fixées observées sur les cinq espèces végétales varie selon l’espèce du Digène : 368 kystes pour F. hepatica, 77 pour C. daubneyi, 20 pour Notocotylus sp. et seulement 4 kystes pour l’Echinostomatidé.
3.1. Distribution des métacercaires en fonction de la vitesse du courant
Le tableau 2 indique la distribution de ces larves dans les deux types de cressonnières par rapport i) à la vitesse de l’eau courante et ii) la longueur de la zone sans macrophyte. Dans les rigoles alimentées par une source à débit lent, le nombre de kystes diminue lorsque la longueur de la zone sans macrophyte augmente. Si l’on considère le cas de F. hepatica, les métacercaires diminuent en nombre jusqu’à 50 kystes lorsque la longueur de rigole sans macrophyte dépasse 3 m. Le même résultat a été observé dans les rigoles alimentées par une source à courant plus rapide, mais la diminution du nombre de métacercaires est plus marquée : de 93 à 4 kystes, respectivement. Malgré cette diminution apparente, la comparaison des moyennes entre les deux types de cressonnières n’a pas montré de différence significative, quel que soir le Digène considéré. Par contre, le nombre de métacercaires est significativement plus faible (C. daubneyi : p < 5 % ; F. hepatica : p < 1 % :) dans les cressonnières parcourues un courant rapide que dans leurs homologues avec un débit plus lent lorsque la longueur de la zone sans macrophyte est supérieure à 3 m.
Tableau 2 : Répartition numérique des métacercaires de quatre Digènes dans 14 cressonnières naturelles de la Haute-Vienne par rapport à la vitesse de l’eau courante et la longueur de la rigole sans macrophyte.
|
Type de source et longueur de la zone sans macrophyte (m) |
Nombre total de métacercaires |
|||
|
Fasciola hepatica |
Calicophoron daubneyi |
Notocotylus sp. |
Echinostomatidé |
|
|
Source à écoulement lent |
||||
|
0,13-0,24 |
89 |
26 |
8 |
1 |
|
1,1-1,8 |
81 |
15 |
4 |
0 |
|
3,1-3,5 |
50 |
7 |
1 |
1 |
|
Source à débit plus rapide |
||||
|
0,15-0,29 |
93 |
21 |
6 |
0 |
|
1,3-1,6 |
51 |
7 |
1 |
2 |
|
3,0-3,2 |
4 |
1 |
0 |
0 |
3.2. Distribution en fonction de la plante hôte
La plupart des kystes de F. hepatica (Tableau 3) ont été trouvés sur N. officinale : 115 au total dans des cressonnières alimentées par un débit d’eau lent et 73 dans celles parcourues par un courant plus rapide. Le nombre de ces larves était moindre sur H. nodiflorum : 63 et 62 kystes par ordre respectif. Sur les trois autres espèces végétales, ce nombre était faible : de 13 à 16 kystes selon l’espèce dans les cressonnières à faible débit d’eau, de 1 à 6 dans les autres. Par rapport à la quantité de feuilles et de tiges échantillonnées pour chaque espèce végétale, le nombre de métacercaires décomptées pour 1 kg de plantes est faible. Les valeurs moyennes relevées chez Callitriche sp. (3,6 ± 0,7 kystes par kg de plantes), H. nodiflorum (3,7 ± 0,6 kystes/kg) et N. officinale (3,8 ± 0,7 kystes/kg) sont assez proches alors que la charge moyenne en métacercaires est significativement plus faible (H4 = 35,52, p < 0,1 %) chez J. effusus (1,9 ± 0,4 kystes/kg) et V. beccabunga (1,0 ± 0,4 kyste/kg).
Tableau 3 : Répartition numérique des métacercaires de quatre Digènes dans 14 cressonnières naturelles par rapport à la vitesse de l’eau courante et l’espèce végétale.
|
Type de source |
Espèce végétale |
||||
|
Nasturtium officinale |
Callitriche sp. |
Helosciadium nodiflorum |
Juncus effusus |
Veronica beccabunga |
|
|
Source à écoulement lent |
|||||
|
Plantes égouttées (kg) |
27,6 |
3,1 |
17,5 |
4,7 |
7,3 |
|
Nombre de métacercaires : |
|||||
|
Fasciola hepatica |
115 |
16 |
63 |
13 |
13 |
|
Calicophoron daubneyi |
25 |
0 |
22 |
0 |
1 |
|
Notocotylus sp. |
7 |
2 |
3 |
0 |
1 |
|
Echinostomatidé |
1 |
0 |
0 |
0 |
1 |
|
Total |
148 |
18 |
88 |
13 |
16 |
|
Source à débit plus rapide |
|||||
|
Plantes égouttées (kg) |
21,1 |
2,9 |
15,9 |
4,4 |
7,7 |
|
Nombre de métacercaires : |
|||||
|
F. hepatica |
73 |
6 |
62 |
5 |
2 |
|
C. daubneyi |
18 |
1 |
9 |
1 |
0 |
|
Notocotylus sp. |
4 |
0 |
3 |
0 |
0 |
|
Echinostomatidé |
0 |
0 |
2 |
0 |
0 |
|
Total |
95 |
7 |
76 |
6 |
2 |
Comme pour les métacercaires de F. hepatica, celles de C. daubneyi (Tableau 3) sont plus nombreuses sur N. officinale que sur H. nodiflorum : 25 au lieu de 22 dans les cressonnières parcourues par un écoulement d’eau lent, 18 au lieu de 9 dans celles avec un courant plus rapide. Sur les trois autres espèces végétales, les kystes sont en très faible nombre à raison d’une seule larve par espèce. La comparaison des charges moyennes en métacercaires n'a pas révélé de différence significative pour N. officinale (0,8 ± 0,3 kystes par kg de plantes) comme pour H. nodiflorum (0,9 ± 0,4 kystes/kg). Les kystes de Notocotylus sp. (Tableau 3) sont nettement moins nombreux : 20 au total, et leur distribution affecte quatre espèces végétales avec 11 d’entre eux sur N. officinale et 6 sur H. nodiflorum, si l’on ne tient pas compte du type de cressonnières. Aucune différence significative n’a été relevée dans la distribution de ces métacercaires, quelle que soit l’espèce de la plante. Les quatre métacercaires de l’Echinostomatidé (Tableau 3) ont une distribution assez hétérogène avec des cercaires qui se sont enkystées sur l’une ou l’autre des plantes appartenant à trois espèces, quel que soit le groupe des cressonnières.
Des métacercaires de Digènes différents ont été observées parfois sur le même spécimen végétal. C’est ainsi que des kystes de F. hepatica et de C. daubneyi ont été identifiés sur N. officinale (4 plantes), H. nodiflorum (1) et V. beccabunga (1). D’autres métacercaires de F. hepatica et de Notocotylus sp. ont également été trouvées sur un spécimen de H. nodiflorum. Enfin, des kystes de F. hepatica, de C. daubneyi et de l’Echinostomatidé ont été observés sur le même plant de N. officinale (résultats non représentés).
3.3. Distribution en fonction du point d’enkystement sur la plante hôte
Tableau 4 : Répartition numérique des métacercaires de deux Digènes dans 14 cressonnières naturelles par rapport au point d’enkystement de la cercaire sur la plante hôte. L’étude porte sur l’ensemble des métacercaires, quel que soit le type des cressonnières. Le nombre total des larves par type de cressonnière et par espèce végétale est indiqué sur le tableau 3.
|
Espèce du parasite et site d’enkystement de la cercaire |
Espèce végétale |
||||
|
Nasturtium officinale |
Callitriche sp. |
Helosciadium nodiflorum |
Juncus effusus |
Veronica beccabunga |
|
|
Fasciola hepatica |
|||||
|
Face supérieure des feuilles |
60 |
5 |
40 |
1 |
9 |
|
Face inférieure |
119 |
17 |
71 |
6 |
5 |
|
Tiges de la plante |
9 |
0 |
14 |
11 |
1 |
|
Calicophoron daubneyi |
|||||
|
Face supérieure des feuilles |
1 |
0 |
0 |
0 |
0 |
|
Face inférieure |
28 |
1 |
24 |
0 |
1 |
|
Tiges de la plante |
14 |
0 |
7 |
1 |
0 |
Le tableau 4 indique la répartition des métacercaires des deux Digènes les plus abondants par rapport au segment végétal sur lequel les cercaires se sont enkystées. Dans le cas de F. hepatica, 219 métacercaires sur un total de 368 (soit 59,5 %) ont été observées sur la face inférieure des feuilles alors que 112 (30,4 %) ont été notées sur la face supérieure et les 37 autres sur les tiges de ces plantes. L’enkystement sur la face inférieure des feuilles est plus net dans le cas de C. daubneyi car 54 kystes sur un total de 77 (70,1 %) y ont été observés tandis que 22 (28,5 %) ont été trouvés sur la partie inférieure des tiges. A l’inverse des deux Digènes précédents, 18 métacercaires de Notocotylus sp. (sur 20) et les quatre kystes de l’Echinostomatidé (résultats non représentés) ont été identifiés sur la face supérieure des feuilles appartenant à quatre espèces végétales. Cependant le faible nombre de ces kystes ne permet pas de dégager des résultats significatifs sur le secteur des plantes sur lequel la plupart des cercaires de ces deux Digènes s’enkystent.
Tableau 5 : Répartition numérique des métacercaires de deux Digènes dans 14 cressonnières naturelles par rapport à la hauteur entre le site d'enkystement des larves et le collet des plantes. L’étude porte sur l’ensemble des métacercaires, quel que soit le type des cressonnières. Le nombre total des larves par type de cressonnière et par espèce végétale est indiqué sur le tableau 3.
|
Espèce du parasite et distance verticale (cm) entre le site d’enkystement et le collet de la plante hôte |
Espèce végétale |
||||
|
Nasturtium officinale |
Callitriche sp. |
Helosciadium nodiflorum |
Juncus effusus |
Veronica beccabunga |
|
|
Fasciola hepatica |
|||||
|
0-5 cm |
0 |
0 |
0 |
0 |
0 |
|
5,1-10 cm |
4 |
0 |
1 |
0 |
0 |
|
10,1-15 cm |
70 |
15 |
31 |
5 |
2 |
|
15,1-20 cm |
95 |
6 |
82 |
11 |
12 |
|
> 20 cm |
19 |
1 |
11 |
2 |
1 |
|
Calicophoron daubneyi |
|||||
|
0-5 cm |
33 |
1 |
24 |
1 |
1 |
|
5,1-10 cm |
9 |
0 |
7 |
0 |
0 |
|
10,1-15 cm |
1 |
0 |
0 |
0 |
0 |
|
15,1-20 cm |
0 |
0 |
0 |
0 |
0 |
|
> 20 cm |
0 |
0 |
0 |
0 |
0 |
La distance linéaire verticale entre le site d’enkystement des cercaires et le collet de leur plante hôte est, de plus, précisée sur le tableau 5. Les sections les plus utilisées par les cercaires de F. hepatica sont comprises entre 10,1 et 20 cm de hauteur, quelle que soit l’espèce végétale : 329 larves sur un total de 368 (soit 89,4 %) se sont enkystées sur l’une ou l’autre de ces deux sections. Au-dessus de 20 cm de hauteur, les kystes de ce Digène ne représentent que 9,4 % (34/368). A l’inverse de F. hepatica, tous les kystes de C. daubneyi ont été observés sur leur plante hôte jusqu’à 10 cm de hauteur. Quant aux deux autres Digènes (résultats non représentés), les sites de l’enkystement sont tous entre 10,1 et 20 cm de hauteur.
3.4. Position des métacercaires par rapport à l’extrémité amont de la cressonnière
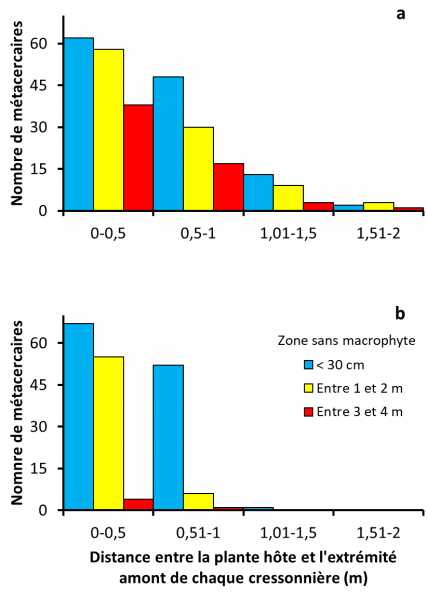
Figure 3 : Répartition des métacercaires de quatre Digènes par rapport à la distance entre la plante hôte et l'extrémité amont de chaque cressonnière : sites alimentés par une source à écoulement lent (3a) et ceux parcourus par un courant d'eau plus rapide (3b). Cette distance est exprimée sous forme de sections longues de 50 cm. Les valeurs sont fournies pour les trois types de longueur que nous avons relevés pour la zone sans macrophyte (légende sur le graphe 3b).
La figure 3 a été construite avec l’ensemble des chiffres que nous avons notés pour les deux types de cressonnières et les trois catégories de longueur pour les zones sans macrophytes. La plupart des cercaires se sont enkystées sur les plantes situées dans la partie la plus en amont de chaque plantation naturelle, généralement sur celles qui poussent sur les 50 premiers centimètres. Aucune métacercaire n'a été trouvée dans la partie aval de chaque cressonnière. De plus, la répartition des kystes sur les plantes varie aussi en fonction de la longueur de la rigole dépourvue de macrophytes. Dans les cressonnières traversées par un courant lent, les métacercaires ont été découvertes sur une distance de 2 m et le nombre de celles-ci diminue progressivement depuis les 50 cm les plus en amont jusqu’à la section des 1,5-2 m (Fig. 3a). Dans celles qui sont parcourues par un courant plus rapide, les métacercaires ont été observées sur une distance plus courte : 1,5 m si la longueur de la zone sans macrophyte est inférieure à 30 cm, 1 m seulement lorsque cette longueur est plus importante. La diminution numérique des métacercaires depuis les 50 cm les plus an amont est aussi plus marquée, en particulier lorsque la longueur de la zone sans macrophyte est supérieure à 1 m (Fig. 3b). Le débit de l'eau courante (H1 = 24,59 ; p < 0,1 %) et la longueur de la zone sans macrophyte (H2 = 15,24 ; p < 0,1 %) ont un effet significatif sur la répartition des métacercaires dans ces cressonnières, alors que l’influence des autres facteurs testés n’est pas nette.
Tableau 6 : Répartition numérique des métacercaires de quatre Digènes dans 14 cressonnières naturelles par rapport à la distance entre la plante hôte et l’extrémité amont des cressonnières. Cette distance est exprimée ici sous forme de sections longues de 50 cm.
|
Type de source |
Espèce du Digène |
Distance entre la plante hôte et l’extrémité amont de la cressonnière (m) |
|||
|
0-0,50 |
0,51-1,0 |
1,01-1,50 |
1,51-2,0 |
||
|
Source à écoulement lent |
Fasciola hepatica |
122 |
73 |
20 |
5 |
|
Calicophoron daubneyi |
28 |
17 |
3 |
0 |
|
|
Notocotylus sp. |
8 |
3 |
2 |
0 |
|
|
Echinostomatidé |
0 |
1 |
0 |
1 |
|
|
Source à débit plus rapide |
F. hepatica |
97 |
50 |
1 |
0 |
|
C. daubneyi |
23 |
6 |
0 |
0 |
|
|
Notocotylus sp. |
4 |
3 |
0 |
0 |
|
|
Echinostomatidé |
2 |
0 |
0 |
0 |
|
Le tableau 6 montre la répartition des métacercaires des quatre Digènes par rapport à la distance entre la plante hôte et l’extrémité amont de chaque cressonnière. Dans les rigoles où l'eau circule avec un débit lent, les cercaires de F. hepatica et celles de l’Echinostomatidé peuvent nager ou être entrainées par le courant jusqu'à 2 m dans la cressonnière avant de s’enkyster sur une plante. Les distances parcoures sont moins élevées pour celles de C. daubneyi et de Notocotylus sp. : moins de 1,5 m de distance après l’entrée de ces cercaires dans la cressonnière. Dans les rigoles avec un courant plus rapide, une cercaire de F. hepatica a pu nager ou être entraînée par le courant jusqu’à la section des 1-1,5 m dans l’une des cressonnières tandis que les cercaires de C. daubneyi et de Notocotylus sp. ne dépassent pas la section des 0,5-1 m.
3.5. Position des métacercaires par rapport à la largeur de la cressonnière
Tableau 7 : Répartition numérique des métacercaires de quatre Digènes par rapport à la position de la plante hôte dans la cressonnière. La largeur de la rigole de drainage est ici exprimée en sections larges de 15 cm.
|
Type de source |
Espèce du Digène |
Nombre de métacercaires par section large de 15 cm |
||
|
0-15 |
15,1-30 |
30,1-45 |
||
|
Source à écoulement lent |
Fasciola hepatica |
87 |
61 |
72 |
|
Calicophoron daubneyi |
21 |
11 |
16 |
|
|
Notocotylus sp. |
10 |
1 |
2 |
|
|
Echinostomatidé |
1 |
1 |
0 |
|
|
Pourcentage |
41,9 % |
26,0 % |
31,8 % |
|
|
Source à débit plus rapide |
F. hepatica |
74 |
19 |
55 |
|
C. daubneyi |
11 |
4 |
13 |
|
|
Notocotylus sp. |
2 |
5 |
0 |
|
|
Echinostomatidé |
0 |
2 |
0 |
|
|
Pourcentage |
47,0 % |
16,2 % |
36,7 % |
|
Le tableau 7 montre la répartition de ces larves par rapport à la position des plantes hôtes dans les rigoles de drainage. Les larves sont plus nombreuses dans les deux secteurs périphériques de la rigole que dans la section centrale, quel que soit le type de cressonnière. C’est ainsi que dans les rigoles à écoulement lent, 41,9 % et 31,8 % des métacercaires ont été observées, respectivement, sur des plantes présentes dans les sections 1-15 cm et 30,1-45 cm, tandis que 26 % seulement ont été notées dans la section centrale. Les chiffres sont encore plus nets dans le cas des rigoles avec un courant plus rapide : 47 % et 36,7 % des métacercaires dans les secteurs périphériques des rigoles et seulement 16,2 % dans le secteur central. Aucune différence significative entre trois sections des rigoles n’a été relevée pour les nombres de métacercaires, toutes les espèces étant confondues.
Discussion
Des métacercaires appartenant à quatre espèces de Digènes ont été identifiées dans les 14 cressonnières étudiées. La liste de ces espèces est en accord avec les données que Rondelaud (2004) et Dreyfuss et al. (2005) ont rapportées dans d’autres cressonnières sur les sols acides du Limousin. La présence des métacercaires de F. hepatica et de C. daubneyi s’explique facilement par le fait que les adultes de ces deux Digènes parasitent souvent les mêmes bovins en France (Szmidt-Adjidé et al., 2000) comme en Espagne (Diaz et al., 2007 ; Iglesias-Piñeiro et al., 2016) ou au Royaume-Uni (Gordon et al., 2013 ; Jones et al., 2017a, b, 2018). Des formes larvaires de notocotyles ont également été rapportées chez G. truncatula en Espagne (Simon-Vicente et al., 1985 ; Manga-González et al., 1994) comme en France (Hourdin et al., 1991 ; Rondelaud et al., 2016). C’est également le cas pour plusieurs espèces d’échinostomes (Vassilev et Kamburov, 1972 ; Kanev, 1985, 1994 ; Skovronsky, 1985 ; Kostadinova, 1995 ; Rondelaud et al., 2016).
Si l’on considère les rigoles avec une zone dépourvue de macrophyte et supérieure à 3 m, la diminution dans le nombre des kystes est plus grande dans les eaux à débit rapide que dans celles à faible courant (Tableau 2). La revue de la littérature sur le problème du parasitisme dans les cressonnières, qu’elles soient commerciales ou naturelles, ne permet pas de fournir une explication pour commenter ces résultats. Cette diminution dans le nombre des kystes peut simplement être due à un nombre plus faible de cercaires émises par G. truncatula dans certaines rigoles car on ne connaît pas le nombre de ces larves que chaque population de limnées libère au départ. Deux autres hypothèses peut-être complémentaires peuvent également être proposées. La première est d'admettre que dans la zone sans macrophyte, de nombreuses cercaires s'enkysteraient sur un support autre qu'une plante de sorte que le nombre de kystes sur les plantes de la cressonnière diminuerait lorsque la longueur de cette zone augmente. La deuxième hypothèse est l’élimination de nombreuses cercaires lorsque la vitesse du courant d'eau circulant dans les cressonnières augmente. Cette dernière supposition s’appuie sur les résultats que nous avons notés dans les plantations à courant assez rapide (Fig. 3b).
Parmi les cinq espèces végétales étudiées, le cresson officinal et H. nodiflorum ont été les plus utilisés par les cercaires des quatre Digènes pour s’enkyster. Ces résultats sont en accord avec les observations que Rondelaud (2004) et Dreyfuss et al. (2005) ont réalisées dans 59 cressonnières naturelles pendant 15 années. D’après ces auteurs, 1165 métacercaires de F. hepatica, 1056 de C. daubneyi et neuf de Notocotylus sp. ont été dénombrées sur N. officinale, tandis que 1097, 222 et deux kystes par ordre respectif ont été observés sur H. nodiflorum. Nos résultats montrent également un nombre plus élevé de métacercaires sur N. officinale que sur H. nodiflorum : 188 kystes de F. hepatica, 43 de C. daubneyi et 11 de Notocotylus sp. au lieu de 125, 31 et 6 kystes par ordre respectif (Tableau 3). A l’inverse de Rondelaud (2004) et de Dreyfuss et al. (2005) qui notent un écart important entre les nombres de métacercaires de C. daubneyi sur le cresson et le faux cresson (1056 kystes au lieu de 222), le nombre de ces kystes est sensiblement identique dans notre étude : 43 sur N. officinale et 31 sur H. nodiflorum. Deux faits peuvent expliquer cet écart entre les nombres de métacercaires sur H. nodiflorum : i) le faux cresson n’est pas présent dans toutes les cressonnières naturelles sur sol acide, et ii) lorsqu’il est présent, son abondance est généralement plus faible que celle de N. officinale (Descubes-Gouilly et al., 1986). A l’inverse des deux plantes précédentes, le nombre de métacercaires est faible sur Callitriche sp. (sauf dans le cas de F. hepatica), J. effusus et V. beccabunga (Tableau 3). Il en résulte que H. nodiflorum et N. officinale seraient les plantes hôtes les plus exploitées par les quatre Digènes pour l’enkystement de leurs cercaires. Cette opinion s’appuie sur les observations de Pécheur (1967). Sur les neuf espèces que cet auteur a proposées aux cercaires de F. hepatica dans les conditions du laboratoire, seules trois d’entre elles ont été largement utilisées par ces larves pour s’enkyster.
Sur les plantes hôtes, la plupart des cercaires de F. hepatica s’enkystent sur la face inférieure des feuilles, tandis que les métacercaires sont en faible nombre sur les tiges. Ces résultats sont en accord avec les observations que Pécheur (1967, 1974), Hodasi (1972) et Dreyfuss et al. (2004) ont rapportées sur les cercaires de ce Digène. D’après Pécheur (1967, 1974), les cercaires s’enkystent principalement sur la face supérieure des feuilles de certaines espèces végétales et sur la face inférieure chez d’autres plantes. Hodasi (1972) note également que l’enkystement des cercaires de F. hepatica s’effectue en grande partie sur les feuilles submergées de Dactylis glomerata Linnaeus, 1753 (graminée) et que les métacercaires se trouvent plutôt sur les feuilles que sur les tiges de la plante. La localisation des métacercaires de F. hepatica sur les sections de la plante comprises entre 10,1 et 20 cm confirme le géotropisme négatif des cercaires de F. hepatica (Pécheur, 1967, 1974). D’après cet auteur, les cercaires auraient aussi un phototropisme négatif car elles sont repoussées par une forte lumière. Cependant, ces larves sont capables de remonter à la surface de l’eau et de s’enkyster en grande partie sur les feuilles ou les parois situées sous la surface de l’eau (Dreyfuss et al., 2004 ; Morley, 2015). Dans le cas de C. daubneyi, notre étude montre une concentration des métacercaires sur les sections les plus basses de la plante et ce résultat est en accord avec le géotropisme positif et le phototropisme négatif que Dreyfuss et al. (2004) ont notés pour les cercaires de ce Digène. Dans le cas de Notocotylus sp. et de l’Echinostomatidé, le faible nombre de métacercaires observées sur la face supérieure des feuilles ne permet pas de dégager un commentaire général sur le segment végétal que choisissent les cercaires de ces deux Digènes pour s’enkyster et les facteurs qui ont une influence sur le choix de ce segment par les cercaires.
Dans les cressonnières situées dans des rigoles de drainage, les plantes qui poussent dans la section la plus en amont (les 50 premiers centimètres) ont été les plus utilisées par les cercaires des quatre Digènes pour s’enkyster, quelle que soit la longueur de la zone sans macrophyte. Le nombre de ces larves sur les plantes a ensuite diminué progressivement en allant vers l’aval, avec une disparition des kystes au-delà de 2 m dans les rigoles à écoulement lent et de 1,5 m lorsque le courant était plus rapide (Tableau 6). Ces résultats sont plus difficiles à interpréter. Les plantes, que l’on trouve dans la section la plus en amont, appartiennent à l’une ou l’autre des espèces étudiées si bien que la préférence des cercaires pour une espèce végétale précise ne peut à elle seule expliquer la concentration de ces larves sur les plantes de cette section. Deux hypothèses peut-être complémentaires peuvent être proposées pour expliquer ce résultat. L'effort, que les cercaires fournissent en nageant sur une longue distance et en particulier dans le cas des cressonnières situées à plus de 3 m des limnées les plus proches, entraînerait la réduction du glycogène et des acides gras présents dans le corps de ces larves si bien que ces dernières s’épuiseraient progressivement et s'enkysteraient sur les premières plantes en entrant dans la plantation. Cependant, un entraînement passif de ces larves en aval sous l’effet du courant, les obligeant à s’enkyster dès qu'elles rencontrent un support végétal, ne peut être complètement exclu.
D’après nos résultats, les métacercaires sont nettement plus nombreuses sur les plantes présentes dans les secteurs périphériques des rigoles (0-15 cm et 30,1-45 cm de largeur) que sur celles poussant dans le secteur central, quel que soit le type de cressonnière (Tableau 7). Les remous qui se produisent lors de l’arrivée courante dans la cressonnière, pourraient être à l’origine de cette répartition, en déviant les cercaires vers les secteurs périphériques des rigoles et en provoquant leur fixation et leur enkystement sur des plantes dans ces secteurs périphériques.
Conclusion
Quatre catégories de métacercaires ont été observées sur cinq espèces de plantes provenant de cressonnières naturelles situées dans des rigoles de drainage superficiel sur sols acides. La plupart de ces kystes ont été trouvés sur les feuilles de N. officinale et, à un moindre degré, sur celles de H. nodiflorum, tandis que les métacercaires sont peu nombreuses sur les trois autres espèces végétales. Les plantes qui poussent dans la section la plus en amont d'une cressonnière sur une rigole de drainage superficiel sont les plus utilisées par les cercaires pour leur enkystement. La vitesse du courant d'eau affecte le nombre et la distribution des métacercaires dans une cressonnière.
L’absence de kystes sur les plantes poussant dans la partie aval de ces cressonnières, c’est-à-dire sur la plus grande longueur de celles-ci, est un premier élément de réponse à la question que plusieurs consommateurs locaux de « cresson sauvage » se posent depuis plusieurs décades. Cependant, il est nécessaire de vérifier ce premier résultat en effectuant des investigations parasitologiques dans des cressonnières naturelles situées dans d’autres collections d’eau (mares, étangs, etc).