La signification des paramètres d'ABRAHAM est la suivante :
- E : excès de réfraction moléculaire (traduit l'effet du volume et de la polarisabilité)
- S : polarité / polarisabilité
- A : acidité par liaison hydrogène (HBA)
- B : basicité par liaison hydrogène (HBB)
- V : volume moléculaire
Pour le 2,3-diméthylphénol :
log P = 0,088 + 0,562 × 0,85 - 1,054 × 0,81 + 0,034 × 0,53 - 3,46 × 0,36 + 3,814 × 1,0569 = 2,52
Pour le 2,4-diméthylphénol :
log P = 0,088 + 0,562 × 0,843 - 1,054 × 0,80 + 0,034 × 0,53 - 3,46 × 0,39 + 3,814 × 1,0569 = 2,42
L'isomère le plus "basique" est le 2,4-diméthylphénol car il a la plus forte valeur du paramètre B
En se rappelant que :
- chaque carbone sp2 apporte un électron au système π
- l'oxygène de la fonction phénol (hybridé sp2) apporte deux électrons
- le méthyle apporte deux électrons (hyperconjugaison)
on obtient les schémas suivants :
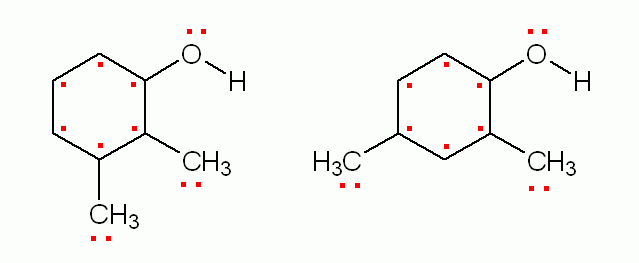
soit 12 électrons π pour chaque composé
En tenant compte du nombre d'électrons π déterminé précédemment, le diagramme d'énergie est le suivant (pour le 2,3-diméthylphénol) :

Note : les deux niveaux à λ = -1,08 et λ = -1,10 sont pratiquement fusionnés sur le graphique.
Calculons l'énergie des électrons π pour chaque isomère :
Eπ(2,3-diMe) =
2 (αC + 2,61 βCC) +
2 (αC + 2,30 βCC) +
2 (αC + 2,16 βCC) +
2 (αC + 1,63 βCC) +
2 (αC + 0,80 βCC) +
2 (αC + 0,75 βCC) =
12 αC + 20,5 βCC
Eπ(2,4-diMe) =
2 (αC + 2,58 βCC) +
2 (αC + 2,32 βCC) +
2 (αC + 2,20 βCC) +
2 (αC + 1,56 βCC) +
2 (αC + 0,91 βCC) +
2 (αC + 0,68 βCC) =
12 αC + 20,5 βCC
Les énergies sont identiques. La méthode de HUCKEL prévoit la même stabilité pour les deux isomères.
-
Il faut considérer l'orbitale HOMO car le composé "basique" se comporte comme nucléophile vis-à-vis de la molécule d'eau.
-
Pour le 2,3-diméthylphénol :
qO = 2 - 2 (0,49² + 0,63² + 0,32² + 0,34² + 0,17² + 0,29²) = 0,064 Pour le 2,4-diméthylphénol :
qO = 2 - 2 (0,53² + 0,43² + 0,53² + 0,36² + 0,06² + 0,31²) = 0,048 La plus forte "basicité" du 2,4-diméthylphénol s'explique donc par :
- une plus forte valeur du coefficient de l'orbitale HOMO sur l'oxygène
- une charge électrique plus faible